CORONAVIRUS
Canarias supera las 200.000 PCR realizadas desde marzo
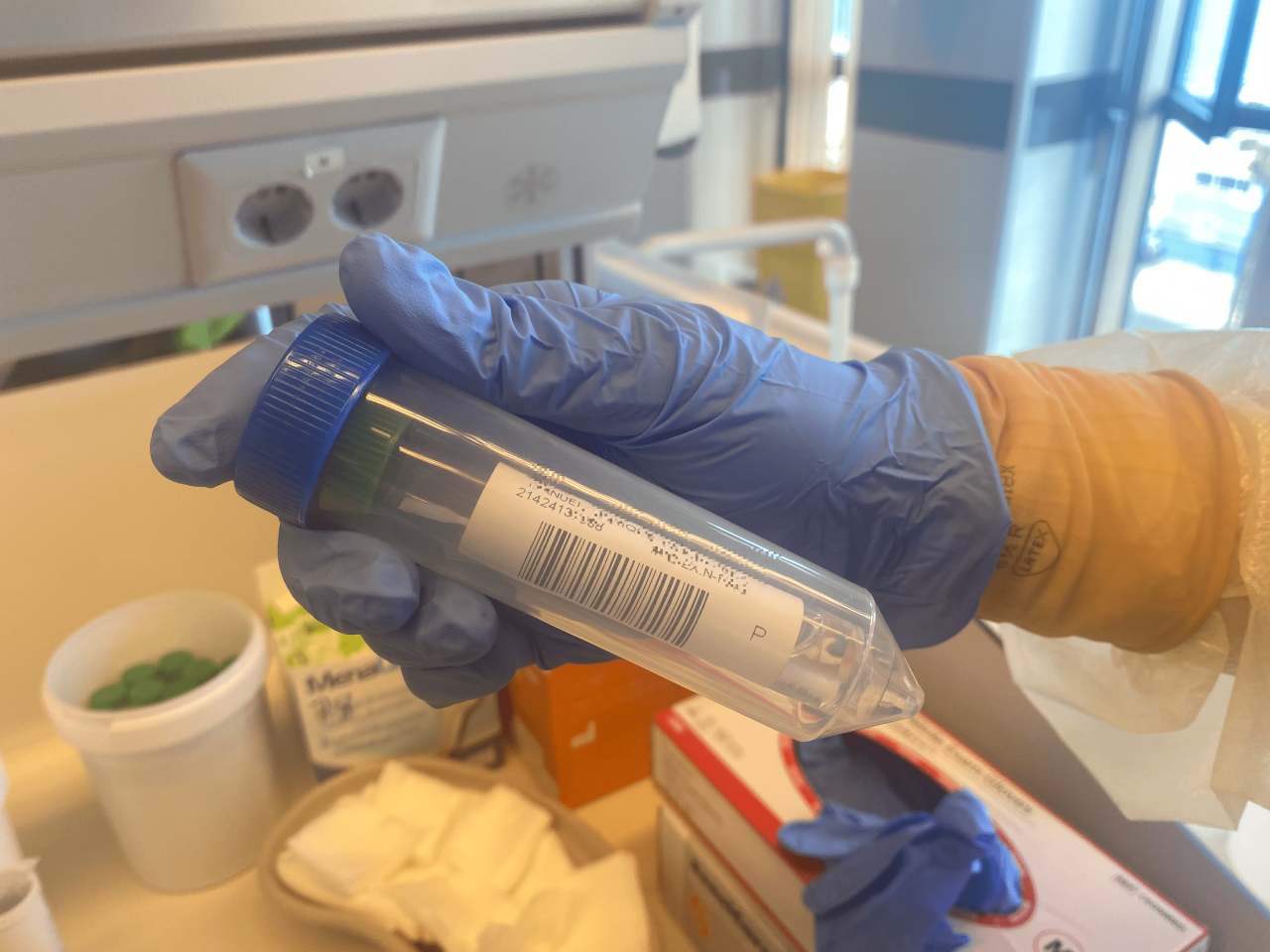
Las pruebas PCR se han convertido en la técnica de referencia y de elección para el diagnóstico de la COVID-19 y en Canarias todos los centros hospitalarios, tanto los cuatro hospitales generales de referencia como los insulares, cuentan actualmente con capacidad para su análisis. Desde el pasado 1 de marzo, las pruebas realizadas en las islas superan las 200.000 y siendo las áreas de salud de Tenerife y Gran Canaria, las dos islas más pobladas, las que concentran el mayor número.
Desde el inicio de la pandemia, todas las islas han recogido muestras para las pruebas PCR, si bien al comienzo la mayoría eran procesadas en los hospitales generales de referencia de las dos islas capitalinas. Sin embargo, en los últimos meses todos los hospitales insulares se han ido dotando de equipos de detección de PCR, como los sistemas Panther, Filmarray o Genexpert.
PCR: técnica y análisis
Desde el servicio de Microbiología del Hospital Universitario Nuestra Señora de Candelaria, la jefa de Laboratorio de Biología Molecular, Julia Alcoba, explica que existen varios tipos de pruebas para el diagnóstico en laboratorio del SARS-CoV-2, entre las que están las PCR, las pruebas de detección de antígenos y las técnicas de detección de anticuerpos (IgM/IgG).
En primer lugar, destacan las PCR (reacción en cadena) que son pruebas de detección de ácidos nucleicos. En la actualidad es la técnica de referencia y de elección para el diagnóstico de la COVID-19, cuyas muestras se obtienen mediante la extracción de material nasofaríngeo y orofaríngeo.
La jefa de Laboratorio de Biología Molecular del Hospital Universitario Nuestra Señora de La Candelaria, Julia Alcoba, explica que la PCR se realiza en laboratorios de microbiología clínica con personal experto en microbiología molecular en un entorno donde se requieren implementar medidas de bioseguridad. Se trata de una técnica utilizada para amplificar secuencias de ADN y se lleva a cabo en dos fases: extracción (una hora aproximadamente) y amplificación de los ácidos nucleicos (entre una y dos horas).
Está basada en la amplificación de fragmentos de ADN mediante ciclos consecutivos de incrementos y bajadas de temperatura, lo que permite, a partir de pocas secuencias iniciales de ADN (pocas copias de material genérico) ampliar a grandes cantidades que pueden ser detectadas mediante fluorescencia. La técnica amplifica ADN, por lo que en el caso de del ARN vírico es necesario primero convertirlo a ADN (por transcripción inversa, RT, reverse transcription) para, a partir de entonces, iniciar el proceso de PCR, llamado RT-PCR.
Para el diagnóstico de confirmación en zonas sin circulación del virus se necesita la positividad frente a dos genes distintos de COVID-19, uno de ellos específico del mismo, o positividad frente a un betacoronavirus más una identificación al menos parcial del genoma del virus COVID-19. En zonas de transmisión comunitaria, se considera suficiente la positividad de la rRT-PCR para un único gen que sea discriminatorio de COVID-19.
El aparataje necesario para la realización del diagnóstico molecular consiste en un sistema de extracción de ácidos nucleicos y en un termociclador donde realizar la PCR. Los procesos se pueden realizar en un único analizador que automatiza ambos. Estos analizadores pueden ser de gran calibre permitiendo analizar un elevado número de muestras. En Canarias hay analizadores de este tipo en todos los hospitales. Entre ellos, está el Panther, el Cobas 6800, Alinity M o el m2000. Otros analizadores también automáticos que analizan muestra a muestra son Filmarray, GenXpert y Liat
Pruebas de detección de antígenos
Tal y como detalla la jefa de Laboratorio de Biología Molecular del Hospital Universitario Nuestra Señora de La Candelaria, Julia Alcoba, las pruebas de detección de antígenos (Ag) se basan en la detección de proteínas virales específicas de SARS-CoV-2 en la muestra, como la proteína N y las subunidades S1 o S2 de la proteína espiga.
La muestra se obtiene del tracto respiratorio, generalmente de exudado nasofaríngeo u orofaríngeo, mediante un hisopo, o de esputo, y se requiere una correcta recogida en el momento adecuado. Según explica, hay poco publicado y, por el momento, los resultados indican baja sensibilidad, por lo que en la actualidad no están aprobados.
Técnicas de detección de anticuerpos (IgM/IgG)
Los tests serológicos se basan en la detección indirecta del virus, a través de la medida específica de los anticuerpos generados por el propio organismo de la persona infectada. Ante el ataque o exposición a organismos ajenos, como los agentes infecciosos víricos, el sistema inmune humano responde desencadenando la producción de anticuerpos que conferirán cierta inmunidad ante posteriores reinfecciones, en un mecanismo análogo al que desencadenan las vacunas.
Las técnicas de detección de anticuerpos son fundamentalmente Enzimoinmunoanálisis (ELISA), Quimioluminiscencia y también inmunocromatográficas. Estas pruebas detectan la presencia de anticuerpos IgM e IgG frente SARS-CoV-2 en una muestra de sangre, suero o plasma.
Se puede diferenciar entre distintos tipos de anticuerpos que se producen en las distintas etapas de la infección: por ejemplo, inmunoglobulinas M (IgM) que se generan al principio, y representan un proceso de infección aguda, y las inmunoglobulinas G (IgG), más abundantes, indicativos de infección primaria o que aparecen como respuesta a la fase aguda de infecciones secundarias.
Para la detección de anticuerpos se dispone de:
a) La inmunocromatografía lateral (lateral flow). Son los denominados kits rápidos, tienen la ventaja de la rapidez y facilidad tanto de obtención de muestra como de uso. No requieren personal especializado, ni para la extracción ni para le realización. Podrían ser utilizados en residencias, servicios de Atención Primaria y urgencias hospitalarias. Hay diferentes tipos de kits rápidos, según detecten IgG e IgM conjunta o separadamente y la sensibilidad y especificidad varían según la casa comercial. No existen estudios comparativos entre los diferentes reactivos comerciales.
b) Las técnicas de ELISA e Inmunoquimioluminiscencia. Requieren de personal especializado para la extracción de la muestra y de equipamiento y personal entrenado para la realización de la técnica. Sin embargo, tienen la ventaja de que permiten conocer la clase y subclase de inmunoglobulinas, así como la cuantificación.
Las técnicas serológicas de detección de anticuerpos realizadas en ensayos de Enzimoinmunoanálisis (ELISA) y Quimioluminiscencia tienen diferentes sensibilidades dependiendo del día en que se haya realizado la muestra desde el inicio de los síntomas. Serían los test adecuados para la realización de estudios cinéticos que permitieran analizar de forma adecuada la respuesta inmunitaria frente al virus SARS-Cov-2 y la toma de decisiones en base a resultados fiables y contrastados. Hay varios sistemas de ELISA y un ensayo de inmunoquimioluminiscencia comercializados.